 |
|
 La combinaison thérapeutique de nifurtimox
et d’éflornithine : Une amélioration thérapeutique contre la maladie du sommeil Par Gerardo Priotto, Investigateur principal, Epicentre, et Ann-Marie Sevcsik, Responsable de la communication scientifique, DNDi |
L’étude clinique de phase III démontre que l’administration combinée de nifurtimox par voie orale et d’éflornithine intraveineuse
(NECT) est un traitement sûr et efficace contre la THA en stade 2 et plus pratique que l’éflornithine en monothérapie.
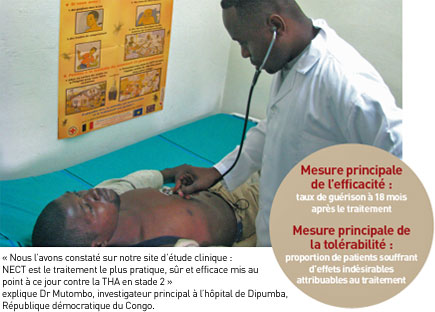 Pourquoi rechercher un traitement combiné contre la THA au stade avancé ? Faire une étude clinique de la combinaison thérapeutique de nifurtimox et d’éflornithine (NECT) se justifiait d’une part en raison du peu de médicaments existants contre la trypanosomiase humaine africaine (THA) en stade 2 et de leurs sérieuses limites et d’autre part, du fait de l’absence de tout développement clinique d’autres médicaments (voir traitements actuels contre la TAH en stade avancé). De la fin des années 1980 à la fin des années 1990, la troisième grande épidémie de THA du 20e siècle a dévasté des communautés rurales entières de l’Afrique subsaharienne – en particulier en Angola, en République démocratique du Congo (RDC), au Sud-Soudan et dans le nord-ouest de l’Ouganda. Face à ces ravages, beaucoup de praticiens de santé publique ont ressenti l’urgence d’améliorer la prise en charge des patients. Les effets secondaires toxiques du mélarsoprol, son efficacité décroissante et l’absence d’alternative réelle rendaient nécessaire la recherche d’une meilleure option de traitement, viable, qui conduirait à la réduction drastique de l’utilisation d’un médicament dangereux et de plus en plus inefficace. NECT émerge comme la plus prometteuse des combinaisons thérapeutiques contre la THA au stade 2 L'Institut de Médecine Tropicale d’Anvers (IMT) en RDC ainsi que Médecins Sans Frontières (MSF) et Epicentre en Ouganda ont réalisé la plupart du travail préliminaire d’évaluation des associations médicamenteuses possibles. Les différentes combinaisons de mélarsoprol, d’éflornithine et/ou de nifurtimox ont été testées au cours de deux essais cliniques en Ouganda. L’association de nifurtimox et d’éflornithine s’est avérée la plus prometteuse des options. Il s’agissait dès lors d’approfondir la recherche afin de déterminer la posologie adéquate et de confirmer la tolérabilité et l’efficacité de l’association.  " Nous avons besoin d’un traitement
plus simple permettant d’envisager la prise
en charge des patients sur le terrain " " Nous avons besoin d’un traitement
plus simple permettant d’envisager la prise
en charge des patients sur le terrain "Epicentre et MSF initient l’étude NECT en République du Congo Encouragée par ces premiers résultats, une équipe d’Epicentre et de MSF initia en 2003 un essai clinique contrôlé randomisé à Nkayi en République du Congo. Cette étude prévoyait d’évaluer l’efficacité et la sécurité d’un schéma d’administration simplifié d’éflornithine sur 7 jours combiné à 10 jours de nifurtimox (NECT) et de la comparer au traitement standard de 14 jours d’éflornithine en monothérapie. Afin de tester statistiquement la non-infériorité de NECT, un minimum de 140 patients devait être recruté pour chaque option de traitement. Malheureusement, cet objectif n’a pas pu être atteint à Nkayi en raison d’une importante réduction d’incidence de la THA dans la région suite aux intenses activités de dépistage et de traitement menées par MSF. Fin 2004, seuls 103 des 280 patients prévus par le protocole d’étude avaient été inclus. DNDi vient en renfort de l’étude NECT En avril 2004, un groupe d’experts - représentant Epicentre, MSF, l’Institut Tropical Suisse (ITS), le Programme spécial UNICEF/PNUD/ Banque mondiale/OMS de recherche et de formation concernant les maladies tropicales (TDR) et DNDi – s’est réuni pour examiner les données cliniques existantes sur l’utilisation du nifurtimox. Les résultats préliminaires encourageants de l’étude NECT y furent présentés. Considérant le bénéfice que constituerait pour les malades un traitement combiné, plus simple d’administration et prouvé efficace, ainsi que les énormes efforts déjà consentis pour recruter plus de 100 patients, les différents organismes décidèrent de s’associer et d’étendre l’essai clinique afin d’assurer l’inclusion d’un effectif suffisant pour fournir des données statistiquement significatives. Durant cette même réunion, DNDi s’engagea à soutenir trois sites d’essai en RDC. Le programme national de lutte contre la THA et l’ITS se sont joints également au projet, aux côtés d’Epicentre et de MSF qui préparaient déjà l’étude à Isangi. Epicentre assurera la coordination médicale, la gestion et l’analyse des données pour l’ensemble de l’étude et travaillera avec tous les partenaires afin de préparer un amendement au protocole d’étude de façon à rendre compte de sa nouvelle dimension multicentrique et son application dans plusieurs pays. Ouverture de trois nouveaux centres d’essai en RDC Le programme national de lutte contre la THA (PNLTHA), DNDi et Epicentre procédèrent à l’évaluation de nouveaux sites potentiels pour l’essai clinique NECT à Isangi, Dipumba et Katanda en RDC. Il s’agissait de déterminer les mesures nécessaires pour mettre ces sites en conformité avec les standards internationaux de bonnes pratiques cliniques (BPC) et renforcer les capacités de recherche clinique. Isangi, dans la province orientale du pays, fut le premier site sélectionné, MSF y ayant débuté un programme de dépistage et de traitement dans l’hôpital local. En juillet 2005, après avoir rénové les installations médicales et le laboratoire et dispensé une formation spécifique au personnel médical, MSF et Epicentre démarrèrent l’essai clinique sur ce nouveau site. En 11 mois, quelques 64 patients furent inclus dans l’étude. En parallèle, deux autres sites d’étude furent identifiés : l’hôpital Dipumba à Mbuji Mayi et le centre de traitement THA à Katanda, distant de quelques 70 km. Après des mesures similaires de rénovation, d’équipement et de formation, les premiers patients furent recrutés en avril et en mai 2006. Sous la coordination médicale d’Epicentre, les équipes de l’ITS et du PNLTHA travaillèrent conjointement dans les deux centres. Des moniteurs cliniques de l’ITS visitèrent régulièrement les trois sites d’essai soutenus par DNDi. 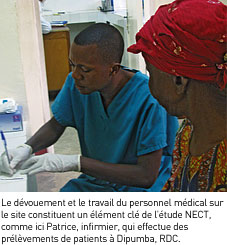 L’essai clinique contrôlé randomisé, conforme aux bonnes pratiques cliniques et avec un excellent taux de suivi post-thérapeutique le démontre : le traitement combiné NECT est bien toléré et efficace L’essai clinique contrôlé randomisé, conforme aux bonnes pratiques cliniques et avec un excellent taux de suivi post-thérapeutique le démontre : le traitement combiné NECT est bien toléré et efficaceEn novembre 2006, l’objectif d’inclure 280 patients dans l’essai clinique était atteint grâce aux 184 participants des trois nouveaux sites soutenus par DNDi en RDC qui étaient venus s’ajouter aux 103 patients déjà recrutés par Epicentre et MSF au centre de Nkayi. Etant donné la période de 18 mois de suivi post-traitement nécessaire à la mesure de l’efficacité, l’analyse des données complètes a finalement pu être achevée en septembre 2008. Les résultats finaux de l’étude démontrent la non-infériorité de l’association thérapeutique NECT en terme d’efficacité et un profil favorable en matière de tolérabilité. Avec un excellent suivi sur 18 mois (93% des patients), le taux de guérison se révèle comparable entre les deux formes de traitement, bien que NECT comporte des avantages importants sur plusieurs indicateurs secondaires. En terme de sécurité, les deux traitements ont été bien tolérés avec un faible taux de mortalité. Ces données démontrent que la combinaison NECT représente la meilleure alternative de traitement de première ligne pour les malades de THA au stade avancé : moins toxique et plus efficace que le mélarsoprol, NECT est en outre plus facile d’utilisation que l’éflornithine en monothérapie. Une demande à l’OMS est actuellement en cours de préparation en vue de l’inclusion dans la liste 2009 des médicaments essentiels du nifurtimox, à être utilisé en combinaison avec l’éflornithine. En parallèle, les résultats finaux de l’étude ont été et seront présentés dans différents forums internationaux, notamment au 17e Congrès international de Paludologie et Médecine tropicale (ICTM), début octobre 2008 à Jeju en Corée du Nord, à la réunion de la Plateforme THA à Brazzaville en République du Congo à la mi-novembre 2008, ainsi qu’à la 57e réunion annuelle de la Société américaine de Médecine tropicale et d’Hygiène (ASTMH) qui se tiendra à la Nouvelle-Orléans, États-Unis, début décembre 2008. Ils feront ensuite l’objet d’une publication au début 2009. 1- Priotto G, Fogg C, Balasegaram M, et al. Three drug combinations for late-stage Trypanosoma brucei gambiense sleeping sickness: a randomized clinical trial in Uganda. PLoS Clin Trials. 2006;1(8):e39. 2 - Checchi F, Piola P, Ayikoru H, Thomas F, Legros D, Priotto G. Nifurtimox plus Eflornithine for Late-Stage Sleeping Sickness in Uganda: A Case Series. PLoS Negl Trop Dis. 2007;1(2):e64. 3 - Priotto G, Kasparian S, Ngouama D, et al. Nifurtimoxeflornithine combination therapy for second-stage Trypanosoma brucei gambiense sleeping sickness: a randomized clinical trial in Congo. Clin Infect Dis. Dec 1 2007;45(11):1435-1442. |
Published by Drugs for Neglected Diseases Initiative - 15 Chemin Louis-Dunant 1202 Geneva Switzerland - Photo credits: DNDi unless otherwise stated - Editor: Sadia Kaenzig - Tel: +41 22 906 9230 - Fax: +41 22 906 9231 - www.DNDi.org